
エボラ治療薬への期待—富山化学が開発のアビガン錠
科学 技術・デジタル 社会 暮らし- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
日本の富山化学工業が創製した抗インフルエンザ薬、アビガン®錠(一般名ファビピラビル)が、西アフリカで猛威を奮うエボラ出血熱の治療薬になるのではないかという期待が高まっている。
世界初、結果良好なら2015年初めにも承認へ
2013年12月にギニアで始まったエボラ出血熱の感染は過去最悪の規模となり、世界保健機関(WHO)は14年8月、西アフリカの4カ国からさらに拡大する恐れがあるとして、「国際的に懸念される公衆衛生上の緊急事態」を宣言した。
病原体となるエボラウイルスは、インフルエンザウイルスと同じく、RNAウイルス(遺伝子としてRNAを含むウイルス)である。80~800nm(ナノ=10億分の1=メートル)の細長い形状をしており、自然宿主としてコウモリが有力とされ、ヒトでは体液を介して感染する。 エボラウイルスに対するワクチンはいまだ存在せず、有効かつ直接的な治療法も確立されていない。だが欧米の研究者らによる動物実験では、アビガンが、インフルエンザ以外に、ウエストナイル熱をはじめとする様々なRNAウイルスに効果があることが示されており、14年に入って、2つのグループがエボラウイルスを感染させたマウスに対する有効性を報告している。
アビガンは、世界に先駆けて14年3月に日本で製造販売承認されたばかりの新薬。その承認は実は制限付きだが、今回のエボラ出血熱の感染拡大で、承認薬として「一定の安全性などが担保できる」と熱い視線を注がれることになった。11月からフランス、ギニア両政府がギニアで臨床試験を実施しており、12月中に結果が明らかになる予定だ。結果が良好ならば年明けにも治療薬として承認される見込みで、世界初のエボラ治療薬として、西アフリカ諸国に日本政府を通じて提供されることになる。
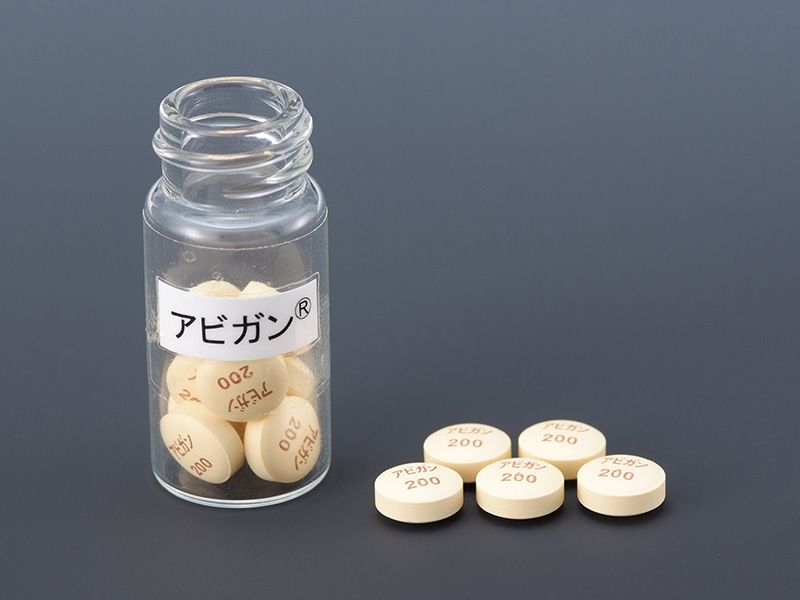 富士フイルムグループの富山化学が開発したインフルエンザ治療薬「アビガン錠」(一般名ファビピラビル)=富士フイルム提供(時事)
富士フイルムグループの富山化学が開発したインフルエンザ治療薬「アビガン錠」(一般名ファビピラビル)=富士フイルム提供(時事)
1990年から開発に着手、1つの核酸誘導体に着目
富山化学は、日本の薬どころとして300年の伝統を持つ越中富山を発祥の地とする中堅の製薬メーカー。同社は1990年、自社の誇る化学合成の能力を強みとして、「抗ウイルス薬開発」を見すえた共同研究を、富山医科薬科大学(現・富山大学)医学部ウイルス学教室の白木公康教授に持ちかけた。
現代では、コンピューターを駆使して標的とするタンパク質に活性を持つ物質を分子設計して合成したり、化合物ライブラリーから網羅的に探索する方法が主流になっているが、当時はまだ移行期で、実際に物質を作っては一つひとつ評価系にかけてスクリーニング(選別)する方法で行われていた。
同社が合成した3万近い化合物を、白木の研究室と富山化学の双方でスクリーニングをする中から、インフルエンザウイルスに対する活性を示したのが、当初「T-705」と呼ばれていた核酸誘導体。白木はその新規性に目を見張った。
既存の研究・特許の網にかからなかった「T-705」
抗ウイルス薬の開発は難しい。様々な病気を引き起こす病原体のうち、細菌などは自ら細胞分裂して増殖するのに対し、ウイルスは自己の複製能力は最小限しか持ち合わせず、感染した宿主の細胞の増殖機構に依存して増える。このため、細胞に害を与えず、ウイルスだけを退治する薬をつくらなくてはならない。
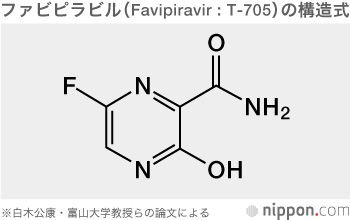 細胞の生存や分裂においては、DNAやRNAなどの核酸は必須で、核酸の構成成分に似た化合物であれば、核酸の働きを阻害する薬になり得るはずだ。こうした発想に立って、ヘルペスウイルスの増殖を抑えるアシクロビル(ゾビラックス®)が開発された。開発にあたった英バローズ・ウェルカム(現グラクソ・スミスクライン)社のジョージ・ヒッチングスとガートルード・エリオンは1988年のノーベル生理学・医学賞を受賞している。
細胞の生存や分裂においては、DNAやRNAなどの核酸は必須で、核酸の構成成分に似た化合物であれば、核酸の働きを阻害する薬になり得るはずだ。こうした発想に立って、ヘルペスウイルスの増殖を抑えるアシクロビル(ゾビラックス®)が開発された。開発にあたった英バローズ・ウェルカム(現グラクソ・スミスクライン)社のジョージ・ヒッチングスとガートルード・エリオンは1988年のノーベル生理学・医学賞を受賞している。
核酸誘導体は抗ウイルス薬として有望視され、続く研究者たちは何千もを合成。日本でも核酸関連物質の製造に強みを持つヤマサ醤油や味の素などが参戦した。白木教授はアシクロビルなどの日本国内での薬理試験にかかわった経験から、「T-705」が、そうした研究や特許の網をくぐり抜けた物質であることに驚かされた。
市場性の壁で、いったんは臨床開発断念
白木教授は漢方で用いられる葛根湯がインフルエンザに効くメカニズム(作用機序)を解明しており、マウスにインフルエンザを感染させて薬効を調べる動物実験の手法を確立していた。T-705はインフルエンザに感染させたマウスで高い治療効果を示したことから、これがインフルエンザ治療薬になるだろうと確信した。動物で効いてもヒトで効かない薬があるため、念のため別の動物を試したが、フェレットでも有効性を示したため、確信は揺るぎないものとなった。
1998年8月に、T-705は物質特許を取得。一連の実験結果は、2000年にICAAC(抗菌剤・化学療法に関するインターサイエンス会議)という大舞台で発表され、02年には国際雑誌に初めて発表された。新薬の開発研究の場合、近年はすべてヒトでの試験研究を終わるまで結果の発表を温存することが一般的になっている。しかしT-705は、まだ新薬の候補物質の段階で、しかも依頼された場合には当該物質の提供義務がある雑誌に報告された。これが後に国際的な評価につながることになる。
実は、この時点で、抗インフルエンザ薬としてザナミビル(リレンザ®)やオセルタミビル(タミフル®)が既に発売されていた。また、欧米では、インフルエンザは服薬せずに1週間安静にして治す病気だ。このため富山化学が海外へのライセンス供与を持ちかけても商談は不調で、同社はT-705を臨床開発へ進めないことを決めた。有望視されていた新薬候補物質であるが、承認のための治験をするとなれば桁違いの費用が必要で、市場性から断念した格好だ。
米研究所にサンプル提供、鳥インフルへの効果で脚光
しかし翌03年、米ユタ州立大学のドナルド・スミー教授からT-705のサンプル提供の依頼があったことで、事態は急展開する。米国では、保健福祉省がバイオテロリズムへの対処も担っており、国立衛生研究所(NIH)では病原体や医薬品開発の基礎研究を行っている。スミー教授は、NIHから研究を依頼されていた。
04年1月、富山化学は、NIH傘下の米国立アレルギー・感染症研究所(NIAID)との間にT-705のサンプル提供契約を締結。スミー教授らが動物実験を続けたところ、05年ごろから東南アジアで猛威を振るっている高病原性鳥インフルエンザ(H5N1)ウイルスに高い効果を示すことが分かった。この結果が06年に報告されると、米国では07年3月から富山化学との提携によってメディベクター社が治験を開始した。国防総省は軍関係者保護目的でこの開発を後押ししており、12年には1億3850万ドルを助成している。
病状進んでも体内のウイルス増殖を阻止
白木教授やスミー教授、そして、東京大学医科学研究所の河岡義裕教授らの研究によって、T-705について様々な知見が明らかになってきた。まずその作用メカニズムが重要で、T-705はウイルス感染した細胞内に入り込み、ウイルスの増殖に必要なRNA ポリメラーゼという酵素(タンパク質)の働きを止め、ウイルスの増殖を阻害することで、RNAウイルスの増殖を阻止する。
リレンザやタミフルはウイルスの体内での増殖は阻止できず、ウイルスが持つノイラミニダーゼという酵素の働きを止め、細胞内で増殖したウイルスが細胞外に出ることを防止する。T-705とは全く異なる作用機序である。
このため、リレンザやタミフルは感染後できるだけ早く、もしくは予防的な服用をする必要があるが、T-705は病状が進んだ状態であってもウイルス量を減少させられる。また、HlN1、H5N1を含む各種のインフルエンザウイルスに対して幅広く抗ウイルス効果を示す。さらに、抗ウイルス薬で最大の問題は耐性を持つウイルスが出現することだが、T-705は、これらの薬に対する耐性株に対しても有効で、耐性が極めて出にくい。また、リレンザやタミフルとの併用で相乗効果を示す。
富士フイルム傘下となり治験が加速
これで一気に期待が高まり、富山化学は日本国内でも07年1月から治験をスタートさせた。しかし残念ながら、さきへ進めるための資金がショートしていた。08年2月、富山化学は医薬品事業への本格参入を目指す富士フイルムに1300億円で買収された。これで調達した約300億円を元に、国内の治験が加速された。
日本では、インフルエンザのパンデミック(世界的大流行)に備え、新型あるいは再興型インフルエンザウイルス感染症が発生し既存薬が無効もしくは効果不十分な場合、T-705を使用可能な状態にしておく意義が評価され、14年3月、「アビガン®」という商品名で世界に先駆けて製造販売承認を取得した。
ただし、動物による安全性試験で胎児に奇形が生じる可能性が認められたことから、承認には厳しい条件が付けられている。直ちに医療用医薬品(処方薬)として販売するのでなく、厚生労働大臣から要請を受けて製造・供給等を行い、新型または再興型インフルエンザウイルス感染症が発生して対策に使用すべきと国が判断した場合に、患者への投与が検討される。妊婦への投与は禁止された。また、有効性を示す臨床試験の成績(主に米国)が限られていたことから、1年以内に追加の薬物試験の結果の提出なども求められている。この間に通常の季節性のインフルエンザへの有効性が示せれば、その効能を追加できる。
日本は新薬を開発できる「数少ない国」
新薬の開発には、最先端の科学に加え、10年以上もの年月と数100億円単位の費用が必要とされる。実は、日本は世界でも新薬を創れる数少ない国である。世界で毎日4000万人以上が服用しているコレステロール低下薬“スタチン”は、ノーベル賞候補ともされる遠藤章氏(東京農工大学名誉教授)が青カビから発見した。またエイズが死病でなくなったのは、熊本大学医学部の満屋裕明教授が発見した薬が化学療法への道を切り開いたからだ。またアフリカでは、大村智氏(北里大学名誉教授)が発見した薬が、熱帯病オンコセルカ症の特効薬として2億人以上を失明から救っている。これ以外にも、日本発で世界に認められている薬はいくつもある。
こうした事実やその開発の歴史は余り知られていないが、日本人はそれを誇りに思ってもいい。そして日本政府も、薬を通じた目に見える国際貢献についても少し検討する余地があるのではないか。
タイトル写真:エボラ出血熱対策のため、西アフリカ・ギニアのゲケドゥに開設された「国境なき医師団」の医療施設=2014年7月9日撮影(The New York Times/アフロ)