Генные механизмы регулирования сна: открытия исследователей из Университета Цукуба
Новости
Наука Технологии- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Прорыв в понимании механизмов сонливости
Миссия Международного института интегративной медицины сна (WPI-IIIS) в Университете Цукуба, которая специализируется на фундаментальных исследованиях сна, добилась грандиозного результата. Впервые в мире благодаря применению амбициозного подхода выявлены два гена, непосредственно связанные с регулированием сна и пробуждения. В ноябре 2016 года эти результаты были опубликованы в электронной версии британского научного журнала Nature.
Почему всем животным, включая человека, требуется погружаться в сон? Какой механизм поддерживает определённую продолжительность сна? Механизмы сна считаются самым большим «чёрным ящиком» неврологии. Но опубликованные результаты проливают свет на эту загадку. «До сих пор никому не удавалось обнаружить гены, имеющие непосредственное отношение ко сну, и нынешняя находка – это прорыв в поисках ответа на вопрос о природе сна, – говорит профессор Янагисава Масаси. – Есть основания полагать, что в дальнейшем этим результатом удастся воспользоваться для лечения нарушений сна».
Многочисленные опыты на мышах
Путь развития традиционной науки – предложение гипотез и их проверка на практике. Сначала выдвигается гипотеза, а затем проводятся многократные наблюдения и эксперименты, в результате которых гипотеза либо подтверждается фактами, либо опровергается, что позволяет приближаться к истине с высокой степенью достоверности. Но загадка сна чересчур глубока. Область сна оставалась слишком неведомым рубежом, чтобы выстраивать хоть сколь-нибудь осмысленные гипотезы.
Для того, чтобы добиться нынешнего результата, профессор Янагисава воспользовался методом, именуемым «прямая генетика», при котором исследователи идут от свойства (фенотипа), наблюдаемого в наследственности, к попытке отыскать отдельные гены, которыми оно обусловлено.
В начале исследования искусственным методом были произведены мыши c разнообразными генетическими отклонениями, в том числе в клетках нервной системы. Вводя самцам мышей вещество, вызывающее изменение генетических данных (этилнитромочевина), в генетический код сперматозоидов вносились случайные нарушения. У следующего поколения мышей – потомства этих особей – исследователи измеряли мозговые волны и снимали электромиограмму, устанавливая таким образом, нет ли у них отклонений сна и бодрствования. Выявив мышей с явно необычными признаками сна – чересчур длительный или наоборот необычайно короткий сон – получали следующее поколение мышей от этих особей. Таким образом подтверждение одинаковых аномалий сна у родителей и их потомства позволяло делать выводы о наследственности этого свойства, после чего определялись гены, общие для всего семейства.
Исследовательская группа профессора Янагисавы и профессора Фунато Хиромасы приблизительно за три года произвела свыше 8 тысяч мышей, тщательно обследуя их на наличие отклонений сна и бодрствования. Процесс требовал много труда, времени и финансовых средств, но учёные терпеливо, шаг за шагом, продолжали выполнять эту кропотливую работу.
 Профессор Янагисава Масаси даёт телевизионное интервью о результатах исследования (фотография предоставлена WPI-IIIS)
Профессор Янагисава Масаси даёт телевизионное интервью о результатах исследования (фотография предоставлена WPI-IIIS)
На следующем этапе исследователи выделили те семейства мышей, у которых было наиболее заметно сокращение продолжительности сна, а также те, у которых была заметно короче продолжительность фазы быстрого сна (REM-sleep), в которой снятся сны. Фактически, во втором поколении мышей количество генетических отклонений превышало 1 000, и задача состояла в отборе генов, имеющих глубокую связь с каждым фенотипом. Затем идентифицированные таким образом гены вводились мышам с использованием новейшей технологии генного редактирования. Тем самым исследователи воспроизводили мышей с генетическим отклонением. Подтверждая проявления фенотипа – сокращения продолжительности сна, а также фазы быстрого сна, учёные получали фактическое подтверждение причинно-следственной связи.
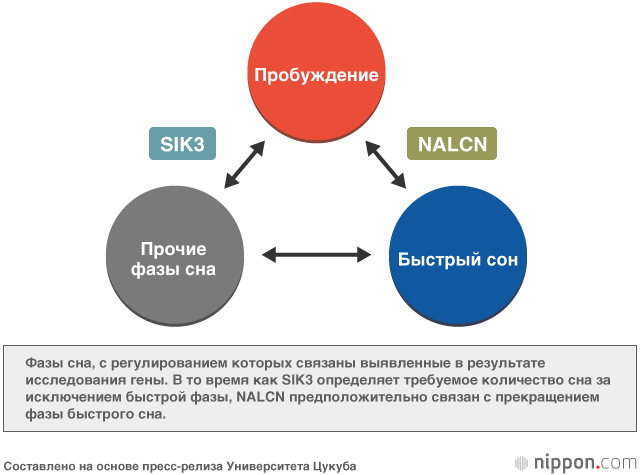
Итогом этого труда стало выявление двух генов – Sik3 и Nalcn.
Семейства мышей с мутацией гена Sik3 во время бодрствования вели себя обычным образом, но сон их был аномально длительным, а время бодрствования – крайне коротким. До сих пор исследователям не удавалось выявить форм передачи на внутриклеточном уровне сигналов, связанных с регулированием количества и качества сна. Теперь же появились основания считать, что сигналом к «сонливости» служит протеинкиназа Sik3. Проследив работу Sik3 в качестве регулятора сна у мух-дрозофил и нематод, исследователи стали полагать, что Sik3 связан с регулированием сна у всех живых существ.
С другой стороны, у мышиных семейств с мутациями гена Nalcn фаза быстрого сна была крайне непродолжительной. Сон подчиняется определённому циклу чередования фаз быстрого и глубокого сна. Под фазой быстрого сна подразумевается состояние, когда тело погружено в сон, но вместе с тем мозг продолжает активно работать. Существует вероятность, что Nalcn отвечает за выработку протеина, который связан с переходом в фазу быстрого сна и обратно, и это позволяет надеяться на то, что находка исследователей впервые приведёт к пониманию механизма этого переключения на внутриклеточном уровне.
Прогресс в разработке лекарства от нарколепсии
В 1998 году профессор Янагисава открыл нейропептид под названием орексин, позволяющий регулировать переключение сна и пробуждения, склоняя весы в сторону бодрствования. С тех пор одним из главных направлений исследований его центра стало практическое применение свойств орексина для создания лекарства от гиперсомнии (нарколепсии). Уже выявлен протеин, служащий рецептором, и теперь надежды на создание соединения, которое послужит лекарством, связывают с агонистом этого рецептора.
Международный институт интегративной медицины сна пригласил к участию в работе на данном направлении профессора Нагасэ Хироси, которому в прошлом дважды удалось добиться успеха в создании лекарств в фармацевтических компаниях. У него получилось синтезировать соединение YNT-185, обладающее высокой растворимостью и даже при низкой концентрации (порядка 10-9mol/L) демонстрирующее эффект в качестве агониста рецептора орексина. Об этом результате исследователи сообщили в 2015 году. Поскольку сообщение ясно описывало структуру YNT-185, в работу разом включились многие фармацевтические компании, взявшиеся за задачу оптимизации структуры с целью создания лекарства. Но профессор Янагисава полон оптимизма: «Мы намерены в течение ближайших двух лет перейти к стадии работы с соединениями-кандидатами для разработки лекарственного препарата, и первыми прийти к финишному этапу – производству лекарства».
Текст: Цукасаки Асако (журналист)
Фотография к заголовку: Крупномасштабная система для единовременного снятия энцефалограммы и электромиаграммы у большого числа мышей (фотография предоставлена WPI-IIIS)
(Статья на японском языке опубликована 3 января 2017 г.)