
طفرة في أبحاث الخلايا الجذعية
علوم تكنولوجيا- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
آخر ما توصل إليه العلم حول الخلايا الجذعية
طُورت الخلايا الجذعية (iPS) أول مرة في عام ٢٠٠٦ من قبل البروفسور ياماناكا شينيا في جامعة كيوتو. وتشكل هذه الخلايا الجديدة إنجازاً مهماً في مجال أبحاث الخلايا الجذعية ولها قدرة علاجية هائلة. يتم إنتاج الخلايا الجذعية من خلال التلاعب الجيني، حيث يتم إدخال أربعة جينات خاصة إلى عينة صغيرة من الخلايا الجلدية مما يسمح لها بأن تتطور إلى خلايا ذات شكل مختلف كلياً وأن تتكاثر تقريباً بشكل غير محدود. ويمكن للخلايا المنتجة بهذه الطريقة أن تتمايز إلى أي نوع من الخلايا أو الأعضاء من بينها العظام والقلب والأعصاب والكبد والدم.
 مخبر مفتوح في الطابق الرابع من مبنى CiRA. تُجرى أبحاث في بيئة بحثية منفتحة بشكل كامل (الصورة مقدمة من CiRA، جامعة كيوتو، يونيو / حزيران ٢٠١٠).
مخبر مفتوح في الطابق الرابع من مبنى CiRA. تُجرى أبحاث في بيئة بحثية منفتحة بشكل كامل (الصورة مقدمة من CiRA، جامعة كيوتو، يونيو / حزيران ٢٠١٠).
إن قدرة الخلايا الجذعية على التكاثر بشكل غير محدود وعلى التمايز إلى أي نوع من الخلايا هو ما يجعل منها خلايا مميزة. حيث هنالك تشابه في الآلية التي تعمل بها هذه الخلايا من طريقة انقسام البيضة الملقحة وتمايزها لتشكل خلايا وأعضاء أو طريقة ترميم الجلد أوالأوعية الدموية بعد تهتكها. كما تمتلك الخلايا الجذعية المستحثة اصطناعياً القدرة على التحول إلى خلايا أخرى والتطور إلى خلايا متعددة وأعضاء من خلال الانقسام والتمايز.
وتتميز الخلايا الجذعية الجنينية (ES) بخواص مشابهة ولكن استخدامها ينطوي على قضايا أخلاقية على اعتبار أنها مأخوذة من أجنة. ونظراً لأن الخلايا الجذعية يمكن أن تتطور من خلايا جسمية (مصطلح عام يطلق على خلايا غير الخلايا التناسلية)، فإنها أقل إشكاليةً بكثير من الناحية الأخلاقية. وتطور طريقة البروفيسور ’’ياما ناكا‘‘ السهلة والفعالة الخلايا الجذعية من خلال تحويل الخلايا الجسمية إلى خلايا متعددة القدرات. وينصب الجهد في الوقت الحالي في محاولة التغلب على قضايا من مثل استجابة الرفض المناعي وتشكل الورم بعد زراعة الخلايا الجذعية. سيكون هناك آمال كبيرة تعلق على الخلايا الجذعية مع نطاق واسع من التطبيقات السريرية لها إذا تمكن الباحثون من التغلب على هذه المشاكل وتم التأكد من أن هذه الخلايا يمكن أن تستخدم بأمان.
ولعل أكثر تطبيق واعد في هذا المجال يتمثل في الطب التجديدي. فمثلا إذا وُجِدَ شخص يعاني من مرض قلبي شديد، فعندئذ يمكن للخلايا الجذعية المطورة من خلايا جلدية لنفس المريض أن تُستحث وأن تنقسم وتتمايز إلى خلايا قلبية بحيث تتم زراعتها مجدداً في قلب المريض. في مثل هذه الحالة، فإن فرصة أن يقوم الجسم برفض الخلايا الجديدة المزروعة ضئيلة لأنها مأخوذة من نفس المريض. كما يمكن استخدام الخلايا الجذعية لإنتاج خلايا أو أعضاء لها تأثير يحاكي أعراض الأمراض المتنوعة التي لا علاج لها، الأمر الذي يمكن أن يؤدي إلى اختراقات في معرفة أسباب تلك الأمراض وتطوير علاجات فعالة.
إنتاج الصفيحات الدموية من خلايا جذعية بشرية
يضم مركز أبحاث وتطوير الخلايا الجذعية المستحثة (CiRA) في جامعة كيوتو أربعة أقسام بحثية هي: قسم علم إعادة البرمجة وقسم نمو الخلايا وتمايزها وقسم التطبيق السريري وقسم علم التحكم بالخلايا. ينصب الاهتمام البحثي في مخبر البروفيسور إيتو كوجي في قسم التطبيق السريري على تقنيات لإنتاج أنواع مختلفة من خلايا الدم من الخلايا الجذعية. فقد نجح البروفيسور إيتو وفريقه البحثي في تطوير طريقة لإنتاج كميات كبيرة من الصفيحات الدموية من الخلايا الجذعية. وعندما يصاب الجلد أو الأوعية الدموية، تعمل الصفيحات الدموية على إغلاق وتغطية الجروح وتلعب دوراً رئيسياً في إيقاف النزيف. ويُطلق مصطلح نقص الصفائح الدموية على الحالة الناجمة عن نقص عدد الصفيحات الدموية. والمعالجة الفعالة تشمل عادة نقل صفيحات دموية بشرية. تفقد الصفيحات الدموية نشاطها الحيوي بسهولة، ولكن باستخدام الطرق الحالية يمكن أن تُحفظ الصفيحات الدموية فقط لأربعة أيام بعد الجمع. بالإضافة إلى عدم توافر الصفيحات الدموية عند الطلب في بعض المناطق. وهناك مشكلة أخرى تتمثل في تشكل أجسام مضادة للصفيحات الدموية (معظم هذه الأجسام المضادة تتشكل كرد فعل لوجود أنتجين كريات الدم البيضاء البشرية ’’HLA(*١)‘‘ الخاص بالشخص المعطي في محضر الصفيحات الدموية) مع تكرار عملية نقل للصفيحات. وهذا يقود إلى خطر احتمال القضاء على الصفيحات الدموية بسرعة نتيجة الرفض المناعي لها.
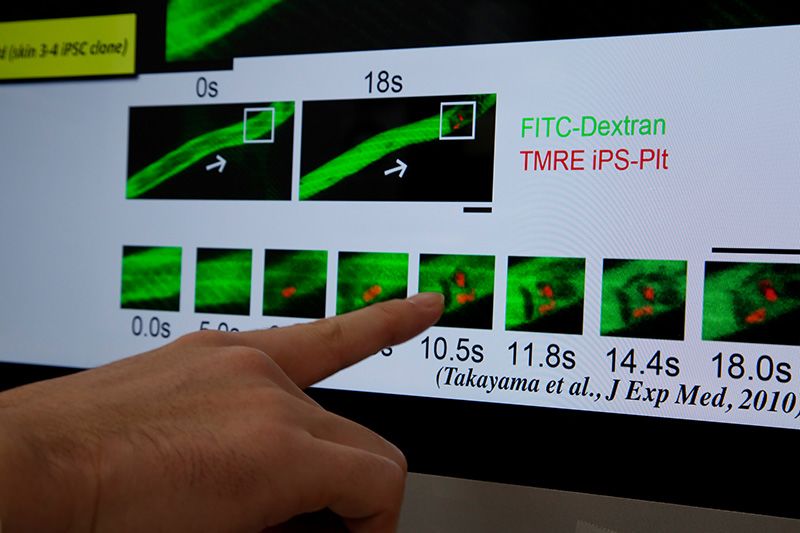 صفيحات دموية منتجة من خلايا جذعية بشرية منقولة إلى فئران. عندما تم إلحاق ضرر ببطانة الأوعية الدموية بواسطة أشعة الليزر، تجمعت الصفيحات الدموية المنتجة من خلايا جذعية بشرية حول الجرح وشكلت تخثرات دموية.
صفيحات دموية منتجة من خلايا جذعية بشرية منقولة إلى فئران. عندما تم إلحاق ضرر ببطانة الأوعية الدموية بواسطة أشعة الليزر، تجمعت الصفيحات الدموية المنتجة من خلايا جذعية بشرية حول الجرح وشكلت تخثرات دموية.
يقول الأستاذ المساعد تاكاياما ناؤويا: ’’إذا كان بالإمكان إنتاج صفيحات دموية بشكل اصطناعي فلن نكون مضطرين للاعتماد على التبرع بالدم بعد الآن، الأمر الذي سيحل مشكلة تأمين الصفيحات. كما أن استخدام الصفيحات المطورة من الخلايا الجذعية المأخوذة من الخلايا الجسمية لنفس المريض سيحل مشاكل الرفض المناعي تلك‘‘. عمل تاكاياما مسبقا كباحث في أمراض الدم ويقول إن أمنيته الكبيرة في تلك الأيام كانت ’’إنتاج صفيحات دموية في الأنابيب‘‘.
عمل تاكاياما على الخلايا الجذعية المستحثة والخلايا الدموية لعدة سنوات. وقد نجح حاليا في إنتاج خلايا نواء وخلايا نقي العظام المسؤولة عن إنتاج الصفيحات الدموية وفي الحصول على الصفيحات الدموية منها. وخلال تجربة على فئران ذات أوعية دموية متضررة بواسطة الليزر، أظهرت صفيحات دموية منتجة من خلايا جذعية بشرية نقلت إلى تلك الفئران قدرتها على العمل بشكل طبيعي، حيث تجمعت في مكان الجرح وشكلت تخثرات دموية لإيقاف النزيف.
التوجه نحو التطبيق السرير
يقول تاكاياما: ’’نحن نعلم أنه هناك خطر تشكل ورم عند استخدام الخلايا الجذعية. ولكن الصفيحات الدموية وكرات الدم الحمراء لا تملك أنوية وبالتالي لا يمكنها أن تتطور إلى أورام. وهذا يعني أنها يمكن أن تستخدم بأمان إذا زرعت بعد التعرض لأشعة وذلك لمنع تكاثر خلايا أخرى. وبهذا المعنى، يمكن القول إن أبحاث الخلايا الجذعية قريبة إلى حد ما من الوصول إلى التطبيق السريري في مجال علم الدم‘‘.
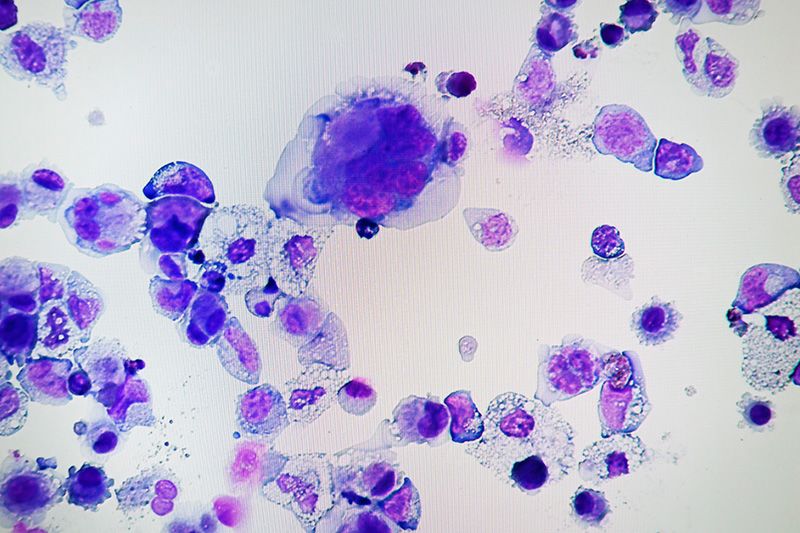 خلايا النواء المنتجة من خلايا جذعية بشرية (الصور ملتقطة من الأستاذ المساعد تاكاياما ناؤويا، مركز CiRA).
خلايا النواء المنتجة من خلايا جذعية بشرية (الصور ملتقطة من الأستاذ المساعد تاكاياما ناؤويا، مركز CiRA).
يتطلب التطبيق السريري العملي استخدام كمية كبيرة من الصفيحات الدموية. يقول تاكايما إن العمل جار لتطوير تقنية لإنتاج صفيحات دموية مستقرة أكثر فعالية. نأمل في المستقبل أن يكون بالإمكان إنتاج خلايا جذعية مكونة للدم، والتي هي مصدر خلايا الدم، من الخلايا الجذعية. إن هذا سيعود بفائدة عظيمة على معالجة الأمراض الدموية التي تفتقر حاليا إلى وجود علاج فعال.
’’تترواح أهداف أبحاثنا في مركز CiRA بين الأبحاث الأساسية إلى المشاريع المشابهة لمثل تلك التطبيقات السريرية. تتمثل طموحاتنا المستقبلية في خلق مخزون احتياطي من خلايا iPS للاستخدام الطبي. كما ان واحداً من أفضل الأمور في مركز CiRA يتمثل في أن الأبحاث تُجرى فيه بنمط متعدد الاختصاصات في مخابر مفتوحة. فأنا مختص بعلوم الدم ولكني أستوحي يوميا الكثير من الأفكار التي تزودني بها تلميحات حول أبحاثي من قبل باحثين زملاء يعملون على أعضاء أخرى أو يجرون أبحاث أساسية‘‘.
 يمكن إنتاج صفيحات دموية من خلايا جذعية جنينية. ولكن الخلايا الجذعية تسمح بإنشاء خطوط خلوية بحيث أن تلك الخلايا تصبح أكثر ملائمة لإنتاج الصفيحات الدموية ويمكن أن تُنقى بسهولة، الأمر الذي يسمح بإنتاج فعال من محضر الصفيحات الدموية.
يمكن إنتاج صفيحات دموية من خلايا جذعية جنينية. ولكن الخلايا الجذعية تسمح بإنشاء خطوط خلوية بحيث أن تلك الخلايا تصبح أكثر ملائمة لإنتاج الصفيحات الدموية ويمكن أن تُنقى بسهولة، الأمر الذي يسمح بإنتاج فعال من محضر الصفيحات الدموية.
ويقول تاكاياما: ’’يمكننا البدء بإنتاج صفيحات دموية بكميات كبيرة بالاعتماد على المعلومات المتوافرة من الخلايا الجذعية التي تنتج صفيحات دموية بشكل فعال‘‘. فقد تم تسجيل التقنيات الأساسية للخلايا الجذعية ببراءات اختراع في أوروبا والولايات المتحدة، كما أن التحضيرات جارية نحو تطوير هذه التقنية بحيث تصبح تجارية. كما نُشرت العديد من الأبحاث حول نجاح تمايز خلايا جذعية بشرية إلى أعصاب وعضلات وأنسجة أخرى. وبدون شك، ستتعلق الآمال في السنوات القادمة على هذا المجال.
(المقالة الأصلية باللغة اليابانية من أوشيجيما بيفويه، الترجمة من الإنكليزية، الصور مقدمة من هانز سوتر)(*١) ^ أنتجين كريات الدم البيضاء البشرية: يتم إنتاج HLA تقريبا في جميع خلايا الجسم وتعمل كمستضد لمعرفة التوافقية النسيجية (تحديد خلايا الجسم نفسه خلال استجابة الجهاز المناعي). يلعب نوع الـ HLA دورا مهما خلال عملية زراعة الخلايا. ويتم التعرف على الخلايا التي لا تتطابق في HLA على أنها أجسام غريبة يتم القضاء عليها من قبل الجهاز المناعي.
العلوم الخلايا الجذعية جامعة كيوتو الطب التجديدي ياماناكا شينيا