
Opdivo, una prometedora inmunoterapia para el cáncer
Ciencia Tecnología Sociedad Vida- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Un nuevo fármaco anticanceroso nacido en Japón
Conocido como “la reina de las enfermedades”, el cáncer lleva cuatro milenios en guerra contra la humanidad. Es un enemigo al que no logramos vencer del todo por más armas que ingeniamos para combatirlo. Solo en 2014, la enfermedad arrebató la vida a 370.000 personas en Japón.
Las células cancerosas son idioblastos (células distintas a las que están a su alrededor) surgidos a partir de células normales, y resultan difíciles de tratar en parte porque alteran el mecanismo que protege la integridad del ser humano como organismo vivo. Las células cancerosas se desarrollan gradualmente sorteando los ataques del sistema inmunológico que protege el organismo y amenazando la vida, y con el tiempo la batalla contra el cáncer va mermando las células inmunitarias.
En 2014 la empresa japonesa Ono Pharmaceutical (con sede central en Chūō-ku, Osaka) presentó el nivolumab (comercializado como Opdivo infusión intravenosa®), un nuevo concepto de anticanceroso que ha generado grandes expectativas como inmunoterapia oncológica revolucionaria. El responsable de tal hallazgo es el investigador de la Universidad de Kioto Honjo Tasuku (actualmente profesor invitado de dicha universidad, y director de la Universidad Prefectural de Shizuoka), que lleva años liderando la investigación en inmunología oncológica a nivel mundial.
El descubrimiento casual del “freno inmunológico”
El primer descubrimiento fue una casualidad. A principios de los años noventa Ishida Yasumasa, entonces estudiante de posgrado del laboratorio de Honjo Tasuku (actualmente profesor asociado del Instituto de Ciencia y Tecnología de Nara), buscaba las moléculas que provocan la muerte celular programada (apoptosis) de las células inmunitarias. En 1992 logró dar con la primera de esas moléculas, a la que bautizó como PD-1 (Programmed cell death-1, Muerte celular programada-1).
Mientras dilucidaba el mecanismo de la molécula PD-1 experimentando con ratones, Honjo descubrió algo insólito: la molécula se expresaba ampliamente en las células inmunitarias activas (células T y células B) y desempeñaba un “papel de freno inmunitario” (inhibidor de puntos críticos de inmunorregulación) con el cual controlaba la respuesta inmunológica. Al anunciar sus resultados en 1999, Honjo intuyó que se podrían aplicar en el tratamiento del cáncer y de enfermedades infecciosas.
Falta de resultados en el primer medio siglo de la inmunoterapia
La inmunoterapia oncológica cuenta ya con medio siglo de historia. El inmunólogo australiano Frank Macfarlane Burnet, ganador del premio Nobel de Medicina en 1960, estableció la “teoría de la supervisión inmunológica del cáncer” en la década de los cincuenta. Esta teoría sostiene que el organismo humano crea unas 3.000 células cancerosas todos los días, pero el sistema inmunitario las elimina y previene la aparición del cáncer. Sin embargo, la teoría de Macfarlane permaneció sin demostrarse durante muchos años.
Los investigadores que compartían la postura de Macfarlane se lanzaron a buscar métodos de tratamiento para inhibir el cáncer mediante el sistema inmunitario, pero nadie logró resultados satisfactorios. A Honjo esta situación le pareció bien lógica. La respuesta inmunitaria se dispara (arranque) al detectar un antígeno, pero no se activa suficientemente si no cuenta con factores coestimuladores (acelerador).
Las inmunoterapias tradicionales consisten en identificar el antígeno específico del cáncer e introducirlo en el organismo para acelerar la respuesta inmunitaria. No obstante, cuando el cáncer ya está presente y los antígenos están muy extendidos por el organismo, con solo añadir unos miligramos de antígeno casi no se obtienen resultados. Si encima existen factores coinhibidores (freno), por más que se pise el acelerador la respuesta inmunológica no se dispara. El tratamiento debe eliminar ese “freno” y reactivar las defensas. Honjo fue el primero en captar este mecanismo inmunológico.
Por otro lado, el investigador estadounidense de la Universidad de Texas James Allison descubrió otra molécula llamada CTLA-4 (cytotoxic T-lymphocyte-associated protein 4, antígeno 4 del linfocito T citotóxico) que desempeñaba el papel de “freno” de las células inmunitarias. En 1996 se logró eliminar por completo tumores en ratones mediante anticuerpos inhibidores de la función del CTLA-4.
Un fármaco creado entre Japón y Estados Unidos
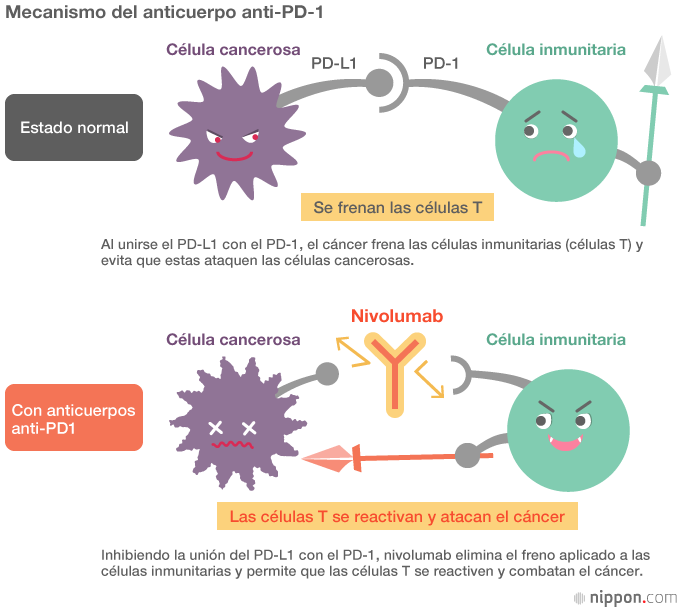
En el año 2000 las investigaciones conjuntas entre la Universidad de Kioto y el Instituto de Genética estadounidense permitieron descubrir sucesivamente el PD-L1 y el PD-L2, dos elementos (ligandos) que se unen específicamente al PD-1. El PD-L1 está presente en la superficie de las células cancerosas y, al unirse al receptor PD-1 de las células inmunitarias, controla la respuesta de las células inmunitarias y acaba con su capacidad para atacar las células cancerosas. Si se inhibe dicha unión mediante anticuerpos anti-PD-1, se elimina el “freno” y las células inmunitarias recuperan la capacidad de atacar el cáncer.
Honjo siguió experimentando con animales y en 2002 publicó unos resultados que ratificaban sus suposiciones: la administración de anticuerpos anti-PD-1 permitía fortalecer significativamente la resistencia al cáncer en ratones. Sus experimentos también permitieron respaldar muchos datos sobre el control de la metástasis y otros aspectos.
A pesar de haber encontrado el camino para poner en práctica sus descubrimientos, como en aquellos tiempos la Universidad de Kioto no era muy ducha en la solicitud de patentes, Honjo Tasuku pidió solicitar la patente de forma conjunta a Ono Pharmaceutical, empresa con la que tenía relación a través de un antiguo profesor. Así fue como en 2002 se realizó la solicitud provisional de la patente para la inmunoterapia basada en el PD-1.
Honjo decidió convertir los anticuerpos anti-PD-1 en un fármaco de inmunoterapia oncológica y propuso su desarrollo a numerosas empresas farmacéuticas. Sin embargo, no obtuvo una respuesta positiva a causa del escepticismo generalizado por parte del sector —al principio incluso por parte de Ono Pharmaceutical— para con la inmunoterapia oncológica. Dando por perdido el mercado japonés, decidió ir a por todas y proponer la colaboración a una pequeña empresa estadounidense, que se mostró muy interesada. Al comunicar la decisión a Ono Pharmaceutical, la empresa aceptó in extremis participar en el proyecto. Este cambio de parecer se debió a que la empresa de biotecnología estadounidense Medarex, que contaba con la patente y la tecnología para fabricar anticuerpos humanos, contactó con Ono Pharmaceutical para buscar la aplicación clínica de los anticuerpos para el PD-1.
En 2006 la Administración de Alimentos y Fármacos (FDA) estadounidense reconoció nivolumab como anticuerpo del PD-1 humano para su uso como nuevo fármaco de investigación, y en el mismo año se iniciaron los ensayos clínicos en Estados Unidos. En 2009 el gigante farmacéutico estadounidense Bristol-Myers Squibb compró Medarex por 2.400 millones de dólares y el proceso de desarrollo del fármaco se aceleró.
Opdivo nace en 2014
Todos los ensayos clínicos que se llevaron a cabo en Estados Unidos tuvieron casos de éxito demostrado. Los ensayos incluyeron pruebas para combatir tumores sólidos y melanomas malignos (melanocarcinomas) de cáncer de pulmón de células no pequeñas, de próstata, de colon, de células renales, etc. En los melanomas y el cáncer de células renales se obtuvo una tasa de respuesta (desaparición del cáncer o reducción superior a una tasa determinada) de casi un 30 %. Los resultados de las pruebas se publicaron en 2012 en la prestigiosa revista de medicina clínica New England Journal of Medicine, y la editorial apuntó que se trataba de “la inmunoterapia con la mejor tasa de respuesta de entre las copiosas inmunoterapias probadas en los últimos 30 años”. En los ensayos incluso se registraron pacientes sin recaídas a largo plazo (en un año o más).
En Japón se han realizado ensayos de fase I (averiguar la seguridad del tratamiento) con pacientes de cáncer de pulmón de células no pequeñas y cáncer de células renales, y se han dado casos de respuesta al tratamiento. Se priorizó el desarrollo del fármaco para tratar el melanoma maligno, el tipo de cáncer con peor pronóstico. Es la primera vez en 20 años que se realizan ensayos de fase 2 para tratar el melanoma en Japón.
La inmunoterapia oncológica con anticuerpos fue elegida por la revista científica estadounidense Science como avance del año (Breakthrough of the Year) en 2013. El nivolumab se aprobó como primicia mundial en Japón con el nombre comercial de Opdivo para tratar el melanoma maligno en julio de 2014, y en Estados Unidos en septiembre del mismo año. En Estados Unidos ya se han finalizado los ensayos clínicos en pacientes con cáncer de pulmón (carcinoma de células escamosas de pulmón en estadio avanzado con historia clínica), y ahora se está llevando a cabo la inspección de prioridad.
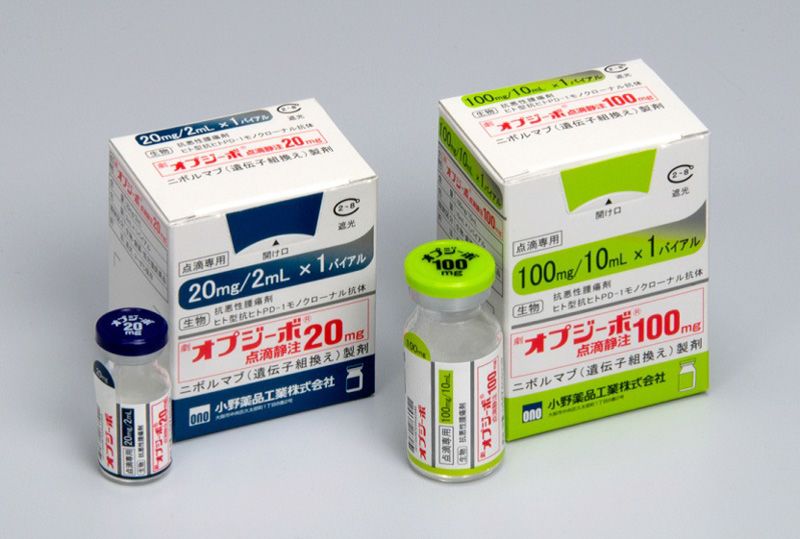 Opdivo, de Ono Pharmaceutical (imagen del comunicado de prensa emitido por la empresa)
Opdivo, de Ono Pharmaceutical (imagen del comunicado de prensa emitido por la empresa)
En la actualidad se siguen realizando ensayos clínicos con el nuevo fármaco para muchos tipos de cáncer, y se prevé ir ampliando su aplicación progresivamente. Además, las empresas farmacéuticas de todo el mundo están desarrollando fármacos dirigidos a los inhibidores de puntos críticos de inmunorregulación.
Bristol-Myers Squibb obtuvo la aprobación de la FDA para el anticuerpo anti-CTLA-4 ipilimumab en 2011 (en Japón se está tramitando su aprobación). A pesar de que tanto el CTLA-4 como el PD-1 funcionan como inhibidores de puntos críticos de inmunorregulación, como cada uno inhibe un aspecto distinto de las células inmunitarias, al usar dos fármacos conjuntamente la tasa de respuesta mejora en gran medida. En 2014 Honjo y Allison fueron los primeros en recibir el Premio Tang de biomedicina (los Premios Tang se crearon como “los Nobel de Asia” y se entregan en Taiwán). La cuantía del premio ascendía a 50 millones de dólares taiwaneses (170 millones de yenes).
Un tratamiento muy ventajoso pero muy caro
Nivolumab presenta tres grandes diferencias respecto a los fármacos tradicionales para tratar el cáncer: 1) es aplicable a todos los tipos de cáncer, 2) tiene pocos efectos secundarios, 3) tiene un efecto continuado incluso en fase terminal y puede readministrarse. Al contrario que los fármacos moleculares dirigidos, que apuntan solo a las moléculas involucradas en la propagación de un tipo de cáncer concreto, los fármacos que inhiben los puntos críticos de inmunorregulación son aplicables a una amplia variedad de cánceres. “Al fin dejarán de usarse los fármacos anticancerosos actuales, y todos los tratamientos consistirán en anticuerpos para PD-1”, vaticina Honjo.
El mayor inconveniente es el aumento del coste del tratamiento. El coste anual medio del tratamiento por paciente aumentará hasta alcanzar los 15 millones de yenes. Sin embargo, los fármacos moleculares dirigidos también tienen costes elevados, no logran evitar del todo la mutación de las células cancerosas y presentan un período de efectividad reducido. No tiene por qué pensarse, pues, que el nivolumab sea demasiado caro, dado que se ha demostrado que elimina total o parcialmente las células cancerosas de muchos de los pacientes en quienes se ha probado. Si en Japón el nivolumab se incluyese en los tratamientos cubiertos por el seguro social, al entrar en la categoría de tratamientos de coste elevado, el coste para el paciente particular podría subvencionarse; el problema es que supondría una carga para el ya mermado presupuesto de la sanidad pública.
El último tema pendiente es que, mientras que en algunos pacientes el resultado es tan bueno que incluso dejan de requerir la administración del nivolumab, en otros no resulta efectivo. Se están considerando distintas medidas para solucionarlo, desde empezar la administración en una fase más temprana de la enfermedad, hasta redefinir los marcadores para evaluar la efectividad del tratamiento.
De la investigación a la aplicación clínica: enlazando la universidad con la empresa
La creación del nivolumab y la planificación del ensayo clínico inicial para validar la adecuación del concepto del producto (prueba de concepto) fueron posibles gracias a la “investigación puente” que permitió trasladar la investigación básica desarrollada por la universidad a la aplicación clínica.
El 1 de abril de 2015 se inauguró la Agencia de Investigación y Desarrollo en Medicina de Japón (AMED), uno de los principales elementos de la tercera flecha del Abenomics (una estrategia de crecimiento para estimular la inversión privada). Empezando por las células iPS, el nivel de la investigación básica japonesa no tiene nada que envidiar al de otros países, pero hasta hace poco el sistema para trasladar los resultados de la investigación a la aplicación clínica era demasiado endeble. La AMED es un organismo análogo a los Institutos Nacionales de la Salud (NIH, por sus siglas en inglés) estadounidenses que permitirá gestionar los presupuestos para I+D médica de forma integrada y promover la aplicación práctica de los frutos de la investigación.
Honjo Tasuku, que tiene experiencia como investigador de los NIH, apunta que “la innovación médica en Japón es un billete sin retorno con medidas insuficientes”. “Necesitamos un sistema mediante el que las empresas farmacéuticas compartan sus beneficios con las universidades; así se logrará formar al personal investigador necesario y crear un círculo positivo que engendre nuevas semillas”. Espero que se logre establecer una auténtica relación de win-win entre las universidades y las farmacéuticas, que tienen el poder de mover el mundo, para empezar a salvar cuanto antes las vidas que hoy en día se pierden a diario a causa del cáncer.
Fotografía del titular: Honjo Tasuku (izquierda) asistiendo a la ceremonia de entrega de los Premios Tang, creados en Taiwán. 18 de septiembre de 2014, Taipéi. (Fotografía cortesía de la Fundación Educativa Tang)Opdivo inmunoterapia para el cáncer inmunoterapia oncológica Honjo Tasuku Ono Pharmaceutical Bristol-Myers Squibb Premio Tang Agencia de Investigación y Desarrollo en Medicina de Japón Cáncer