臓器は“つながり”の中で生きる:iPS細胞から作るオルガノイド研究の最前線
健康・医療 科学- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
臓器移植の壁を越える試み
重い病気や事故などで臓器の機能が低下した人にとって、移植は命をつなぐ最も有力な手段だ。しかし、日本臓器移植ネットワークによれば、日本で移植を希望する患者約1万6000人に対して、提供臓器は圧倒的に不足しており、移植を受けられる人は年間500〜600人程度。待機期間は長期化し、その間に命ついえる人も少なくない。
こうした医療の現状を根本から変える可能性を秘めるのが、iPS細胞から臓器の一部を作り出す「オルガノイド(ミニ臓器)」の研究だ。
iPS細胞とは、皮膚や血液といった体の細胞に少数の遺伝子を加えて初期化し、さまざまな細胞へと変化できる状態へと戻した細胞のこと。これを用いて適切な培養条件下で分化させると複数の細胞が自己組織化し、臓器の構造を持つ小さな立体組織、オルガノイドが形成される。
iPS細胞から臓器を立体的に作る
横浜市大医学部を卒業してわずか2年目の研究者だった武部は2013年、iPS細胞から肝細胞に、血管の細胞、細胞同士をつなぐ間葉系細胞を組み合わせ、発生初期の肝臓に相当する「肝芽(かんが)」と呼ばれるオルガノイドを作り出した。

iPS細胞から作成した世界初の肝臓オルガノイド=2013年7月、横浜市立大学(共同)
わずか4ミリほどの肝芽を、肝不全のマウスに移植すると自律的に血管網や肝機能の一部を持つ状態に成長し、マウスの生存率が大幅に向上した。iPS細胞から作った組織が体内で機能することを示したこの成果を英科学誌ネイチャーで発表すると、世界的に注目された。
武部教授はこう話す。
「この成果について、重要な点が二つあると思っています。一つは、臓器再生を考えるときに、単一の細胞だけでなく、複数の細胞が関わるより複雑な仕組みが重要ではないかという問題提起ができたことです。もう一つは、私たちが作った肝芽が、胎児の体内で形成されるごく初期段階の肝臓に相当する組織だったことです。こうした未熟な組織を体内に移植すれば治療につながる可能性があるという考え方を示せたことが、大きなポイントでした」
移植医療に限界を感じ再生医療へ
武部教授が医療の道を志したきっかけは、小学校3年生の時に父親が脳出血で倒れたことだった。一時は危険な状態に陥り、子どもながらに人の死を意識し、何度も不安な気持ちに襲われたという。奇跡的に一命をとりとめ、社会復帰するまでに回復していく姿を見て、「人の命を救う仕事」を意識するようになった。進学先に選んだのは横浜市立大学。「横浜市民割引の特典にひかれて」と笑う。
大学では、当初、肝臓移植をする外科医を目指した。高校で親しかった後輩の父親が生体肝移植を受けたものの、数カ月後に亡くなってしまったのを目の当たりにした体験が影響している。しかし、移植医療に関わるなかで、移植用臓器の絶対的な不足という現実に直面する。
「移植は根本から病気を治す医療だと、シンプルに治療効果に魅力を感じて志しました。ただ臓器提供が限られるなかで、実際の現場では待機患者のすべてを救えるわけではない。医師が病気を治しているというより、救える人を選んでいるという感覚があり、すごくつらいなと思いました」
そこで、臓器を作る再生医療の研究へと進んだ。当時、再生医療研究には万能細胞である胚性幹細胞(ES細胞)が使われていた。受精卵の初期胚から作るES細胞は生命倫理上の問題が指摘されており、横浜市大では使用が認められていませんでした。そこにiPS細胞が登場して、私のような研究ビギナーでもアクセスできるようになったんです。移植に代わる治療法として何が最適かはまだ分かりませんが、細胞から臓器を作り出す再生医療のアプローチが一つの道ではないかと思っています」
臓器は“つながり”の中で生きる
武部教授の研究は、臓器を単独の組織としてではなく、体内で他の臓器とつながる構造として捉える方向へと進んでいった。
2019年には、武部教授らはヒトのiPS細胞から肝臓・胆管・膵臓が連続して形成される「ミニ多臓器」の作製に成功した。肝臓は本来、胆管を通じて膵臓などとつながった構造の中で発生し、機能している。チームはこうした臓器が生まれる発生環境を再現した。
さらに、2025年にはヒトの実際の肝臓に近い構造を持つ肝臓オルガノイドの作製に成功した。肝臓では、栄養を分解する細胞や栄養を作り出す細胞など、役割の異なる細胞が働きを分担している。このプロジェクトでは、こうした細胞の多様性と配置の違いを再現し、治療への応用へと一歩近づいた。
「多くの生命科学の取り組みでは、要素を分解してシンプルにすることで因果関係を明らかにしようとします。例えば肝臓なら肝細胞だけを取り出して調べるのですが、私のアプローチはむしろその逆です。細胞や組織を組み合わせて、より複雑な状態をつくってみる。実際、肝臓は幹細胞だけでできているわけではないし、体の中で単独で存在しているわけでもない。胆管や膵臓、腸とつながった構造の中で機能しています。そうした“つながり”全体を視野に入れることが大切だと考えています」
オルガノイドを使った治療へ
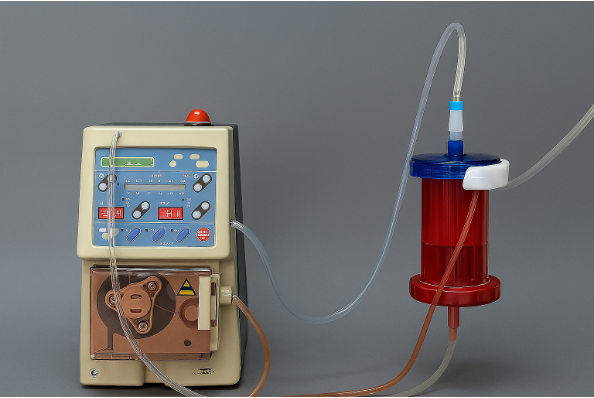
そして現在、研究は実用化に向けた段階へと進みつつある。その一例が、肝臓オルガノイドを利用した「体外循環型装置」の開発だ。人工透析に近いイメージで、急激に肝機能が低下した患者の血液を体外に循環させ、その過程でオルガノイドに肝臓の働きの一部を担わせ、低下した肝機能を一時的に補助する仕組みである。
装置には、iPS細胞由来の微細な肝臓オルガノイドを約1000個まとめて、球状の小さなカプセル「人工いくら」に入れる。これをカートリッジに数百個詰めてそこに血液を通し、肝臓の解毒や代謝といった機能の一部を代替する。
ラットを用いた実験では、生存率の改善が確認された。急性肝不全などで急激に肝機能が低下した患者が、自力で回復するまでの危機的な期間を乗り越えるための治療法として期待され、早ければ2027年後半にも臨床試験が始まる。
「肝臓は何百もの代謝をつかさどる臓器であり、体外循環装置がどの機能をどこまでカバーできるのかは今後の検証が必要です。ただ、この装置には2つの効果があります。肝機能を一時的に補う役割に加え、若い肝臓組織から分泌される成分が病気の肝臓に働きかけ、回復や再生を促す力があることも分かってきました」
生命の力を引き出す研究
肝細胞に血管、間葉系の細胞を組み合わせ、肝臓から胆管、膵臓へと“つながり”を作る。武部教授の前例のないアプローチは、なぜここまでうまくいっているのか──。
「生命がもともと持っている力を信じる、というのが前提です。受精卵という一つの細胞から約10カ月経てば人間が生まれるわけですよね。つまり、適切に環境を整えれば、細胞は自分たちの力で発生していくんです」
この考え方は、研究の現場でも具体的に生かされている。
「細胞を観察していると、思いがけない変化や兆しが現れることがあります。研究目的と違うものとして無視されがちですが、私はそこに意味があるのではないかと考えます。その兆しをどう導けるかを考えながら、条件を整え生命が本来持っている力を引き出すようにしています」
現段階では、胆管から十二指腸へと続く胆汁の排出経路を再現できないことなどから、武部教授のオルガノイドの応用は急性疾患への一時的な治療に限られると考えられている。しかし、肝臓・胆管・膵臓から十二指腸へと至る「胆汁の出口」まで含めたつながりを再現できれば、慢性疾患の治療へと道が開ける可能性がある。
「“つながり”とは、単に臓器同士が直接つながることだけではありません。体の中では血管などを通じてさまざまな臓器が影響し合っています。こうした体全体のシステムのやり取りをどう再現するかが課題です。もし次に私たちが大きな成果を報告できるとすればこの領域になるので、楽しみにしていただけたらと思います」
臓器を「作る」だけでなく、「つながり」まで再現する──。iPS細胞由来オルガノイドによる再生医療は、いま次のステージへと踏み出そうとしている。
取材・文:杉原由花
編集協力:株式会社POWER NEWS
バナー写真・本文中写真:東京科学大学湯島キャンパスにて横関一浩撮影