
Иммунотерапия онкологических заболеваний: препарат Opdivo компании «Оно якухин»
Наука Технологии Общество Жизнь- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Новый препарат для лечения рака, созданный в Японии
На протяжении четырёх тысячелетий человечество ведёт борьбу с раком — заболеванием, которое называют «императором всех недугов». При всех средствах и методах, которые появились в распоряжении людей к настоящему времени, мы всё ещё далеки от победы. Только в 2014 году онкологические заболевания унесли жизни приблизительно 370 тысяч японцев.
Одна из трудностей борьбы с раком состоит в том, что раковые клетки, будучи девиантными клетками, возникшими из нормальных клеток человеческого организма, используют тот механизм, который обеспечил процветание человека как биологического вида. По мере того, как раковые клетки множатся, избегая атак иммунной системы, служащей оружием биологической защиты организма, иммунные клетки истощаются длительной борьбой с раковой опухолью.
В 2014 году в Японии появился созданный на основе новой концепции препарат для борьбы с раком — nivolumab (патентованное товарное наименование — Opdivo для внутривенного капельного вливания). Его производит фармацевтическая компания «Оно якухин когё» (Ono Pharmaceutical Co., Ltd.), штаб-квартира которой расположена в районе Тюо города Осака. На nivolumab возлагают большие ожидания как на действенное средство лечения онкологических заболеваний методом иммунотерапии. Главную роль в создании этого инновационного лекарства сыграл Хондзё Тасуку из Киотского университета, который на протяжении долгих лет является одним из лидеров мировых иммунологических исследований (в настоящее время Хондзё Тасуку — ректор Общественного университета Сидзуока).
Случайное открытие функции «торможения иммунной системы» нашло применение в лечении онкологических заболеваний
Первое открытие было случайным. В самом начале 1990-х годов Исида Ясумаса, в то время доцент аспирантуры Киотского университета (ныне адъюнкт-профессор Института передовых научно-технических исследований Нара), в исследовательской лаборатории Хондзё вёл поиск молекул, вызывающих запрограммированный иммунной системой процесс гибели (апоптоз) клеток. Первая из таких молекул, открытая в 1992 году, получила название PD-1 (аббревиатура от Programmed cell death-1).
Выяснение механизма её действия путём опытов на мышах привело к неожиданному выводу. Были получены доказательства того, что PD-1, широко проявляясь в активизированных иммунных клетках (T-клетки и B-клетки), способен вызывать подавление иммунной реакции, выступая в качестве «тормоза иммунитета» (молекулы-контролёра иммунной реакции). В 1999 году, одновременно с публикацией доклада о полученных результатах, Хондзё высказал интуитивную догадку о возможности применения этого механизма для лечения инфекционных и онкологических заболеваний.
Иммунная терапия: рождение идеи и полвека неудач
Со времени появления идеи иммунотерапии онкологических заболеваний прошло уже более полувека. Удостоенный в 1960 году Нобелевской премии австралиец-иммунолог Фрэнк Мафарлейн Бёрнет в 1950-х годах выдвинул гипотезу об «иммунном надзоре за образованием злокачественных опухолей». Суть её состоит в том, что ежедневно в человеческом организме образуется порядка трёх тысяч раковых клеток, но иммунная система предотвращает развитие опухолей, ликвидируя эти клетки. Однако на протяжении долгого времени гипотеза оставалась неподтверждённой.
Поддержавшие теорию исследователи занимались разработкой методов лечения, подавляющих раковую опухоль силами иммунной системы. Однако результаты их трудов вряд ли можно считать существенными. Хондзё считал это вполне естественным. При реагировании иммунной системы идентификация антигена служит своего рода «зажиганием», инициацией. Но в отсутствие должного ко-стимулирования («акселератора»), система не активизируется в достаточной мере.
Прежние методы иммунотерапии онкологических заболеваний предполагали выявление специфичных раковых антигенов и активизацию иммунной системы путём их введения в организм. Но в условиях наличия в организме раковой опухоли, когда в огромном количестве присутствуют и антигены, незначительное — несколько миллиграммов — введение антигенов даёт слабый эффект. Более того, в условиях, когда действует негативное ко-стимулирование («торможение»), сколько бы ни вводилось «акселератора», иммунного ответа не происходит. Будучи одним из лучших иммунологов, Хондзё прекрасно понимал, что ключевой задачей на пути к излечению является реактивация иммунитета посредством снятия «тормоза».
В то же время в США исследователь Джеймс Эллисон из Техасского университета обнаружил ещё один вид молекул, служащих «тормозом» для иммунных клеток — CTLA-4 (антиген 4 цитотоксических Т-лимфоцитов). В опубликованном в 1996 году докладе сообщалось о том, что с помощью антител, препятствующих функционированию CTLA-4, удалось добиться исчезновения раковой опухоли у мышей.
Совместные японско-американские исследования подтвердили: находка может служить терапевтическим средством
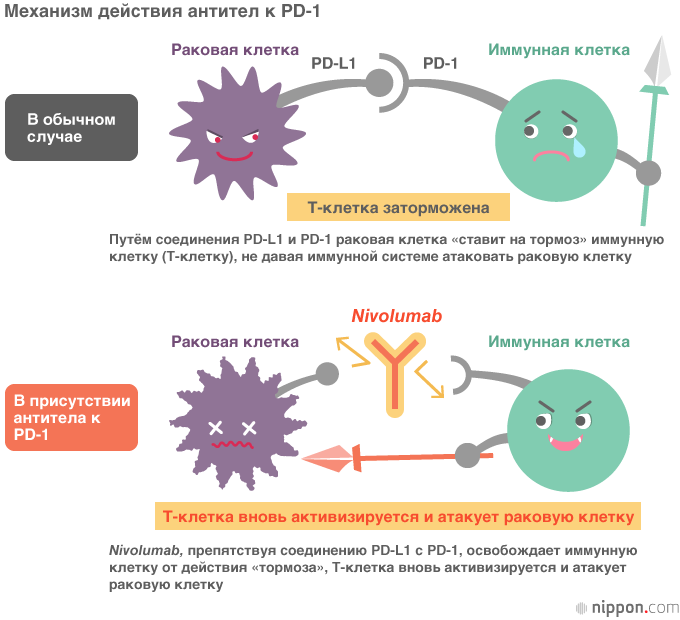
В 2000-м году в ходе совместных исследований Киотского университета с американским Институтом генетики (Genetics Institute, Inc.) и другими партнёрами были одно за другим выявлены два вещества-лиганда — PD-L1 и PD-L2, которые связывают именно PD-1. Находящийся на поверхности раковой клетки PD-L1, связываясь с PD-1 — рецептором иммунной клетки — подавляет её реакцию, нейтрализуя способность атаковать раковую клетку. Если же воспрепятствовать этому соединению с помощью антител к PD-1, «тормоз» иммунной клетки будет ликвидирован, и она вновь обретает возможность атаковать раковую клетку.
В лаборатории Хондзё провели практические тесты на животных. Как и надеялись экспериментаторы, введение антител к PD-1 значительно повысило способность мышиного организма бороться с раковыми клетками. Научная статья с описанием результатов была опубликована в 2002 году. В ходе различных опытов были также подкреплены данные о подавлении пересаженных метастазов и т. д.
Параллельно шёл поиск путей практической реализации полученных знаний. Поскольку в то время Киотскому университету не хватало практического опыта в процедурах патентной регистрации, Хондзё обратился с предложением о совместной подаче заявки на регистрацию в компанию «Оно якухин», где у него был знакомый ещё с преподавательских времён. В 2002 году была подана заявка на получение патента на метод лечения с использованием PD-1.
Будучи уверен, что антитела к PD-1 послужат средством для лечения онкологических заболеваний, Хондзё обратился с предложением о разработке лекарства к многим фармацевтическим фирмам. Поначалу везде, в том числе и в компании «Оно якухин», идею иммунотерапии онкологических заболеваний восприняли скептически. На предложение никто не откликнулся. Получив отказ в Японии, Хондзё обратился к венчурным предприятиям в США, которые отреагировали весьма позитивно. Когда Хондзё сообщил об этом компании «Оно якухин», там в последний момент согласились на проведение разработки собственными силами. Предположительно, истинная причина смены намерений состояла в том, что одно из биотехнологических предприятий США, Medarex, которое располагало технологией производства антител человеческого организма и соответствующими авторскими свидетельствами, обратилось к «Оно якухин», сообщив о желании клинического применения антител к PD-1.
В 2006 году nivolumab в качестве антител человеческого организма к PD-1 был одобрен Управлением по контролю за продуктами питания и лекарственными средствами США как новый препарат для исследовательских целей. В том же году в Соединённых Штатах приступили к его клиническим испытаниям. В 2009 году крупный американский производитель фармацевтической продукции Bristol-Myers Squibb приобрел компанию Medarex за 2,4 млрд долларов, после чего разработка лекарства стала продвигаться ускоренными темпами.
2014 год: рождение лекарственного препарата Opdivo
В ходе испытаний в США средство было опробовано при лечении немелкоклеточного рака лёгких, рака предстательной железы, рака толстой кишки, почечно-клеточного рака и других форм солидных раковых опухолей, а также злокачественной меланомы. Эффективность подтвердилась во всех перечисленных случаях. При лечении злокачественной меланомы и почечно-клеточного рака процент положительного клинического ответа составил почти 30% (показатель доли пациентов, у которых опухоль полностью исчезла либо уменьшилась до размера менее определённой доли от первоначальной величины). Результаты практических испытаний были опубликованы в 2012 году в наиболее влиятельном издании в области клинической медицины New England Journal of Medicine, редакция которого в своей колонке охарактеризовала их в качестве «самого успешного положительного клинического ответа среди средств иммунной терапии рака из всех многочисленных попыток последних 30 лет». У некоторых пациентов рецидивов не наблюдалось на протяжении длительного времени — более одного года.
В Японии компания «Оно якухин» провела первую фазу испытаний, в ходе которой исследуется безопасность препарата, на пациентах с почечно-клеточным раком и другими формами опухолей. В ряде случаев наблюдалась полная ремисссия. Наиболее далеко разработку удалось продвинуть в лечении меланомы — диагноза с наименее утешительными прогнозами. Фактически, вторая фаза испытаний препарата от меланомы проводится в стране впервые за последние 20 лет.
В 2013 году иммунотерапия рака с применением антител была выбрана американским научным журналом Science в качестве «революционного открытия года». В июле 2014 года Япония стала первой страной, где nivolumab в форме лекарственного препарата под названием Opdivo был одобрен в качестве лечебного средства от меланомы, а в сентябре он был одобрен в Соединённых Штатах Америки. В этой стране завершили испытания, связанные с лечением рака лёгких (прогрессирующий плоскоклеточный рак лёгкого с историей лечения), и уже рассматривают вопрос утверждения в ускоренном порядке.
 Opdivo производства компании «Оно якухин» (из корпоративного пресс-релиза)
Opdivo производства компании «Оно якухин» (из корпоративного пресс-релиза)
Поскольку сейчас препарат проходит клинические испытания на многочисленных видах онкологических заболеваний, можно надеяться на расширение области его применения. Кроме того, крупные мировые фармацевтические компании ведут разработку многочисленных лекарственных препаратов, использующих тот же самый механизм иммунной системы.
В 2011 году одобрение Управления по контролю за продуктами питания и лекарственными средствами США получил препарат компании Bristol под названием Ipilimumab, использующий антитела к CTLA-4 (сейчас рассматривается заявка на его одобрение в Японии). Как и PD-1, будучи молекулами-контролёрами иммунной системы, CTLA-4 ослабляют другой аспект иммунитета, и объединённое применение двух этих лекарственных средств позволяет серьёзно улучшить показатель положительного клинического ответа. В 2014 году Хондзё и Эллисон были удостоены первой премии в области биофармацевтики — учрежденной на Тайване Премии Тан, которую прозвали «азиатской Нобелевской премией» (премиальная сумма составляет 50 млн тайваньских долларов, или приблизительно 170 млн японских йен).
Высокая стоимость лечения при незначительных побочных эффектах и множестве других преимуществ
В сравнении с предшественниками, nivolumab обладает тремя отличительными особенностями: (1) разновидность рака не имеет значения, (2) побочные эффекты немногочисленны, (3) препарат эффективен даже при начале лечения на последней стадии развития болезни и допускает многократное применение. В отличие от молекулярно нацеленных препаратов, чьё воздействие ограничено молекулами, связанными с размножением строго определённых видов раковых клеток, препараты, блокирующие иммунный контроль раковых клеток, являются эффективным средством лечения обширного спектра онкологических заболеваний. Сам Хондзё предсказывает: «В конце концов, лекарства на основе антител к PD-1 заменят все нынешние противораковые препараты».
Главным недостатком является дороговизна лечения. Средняя годичная стоимость лечения пациента достигает приблизительно 15 млн йен. Вместе с тем, прочие лекарства-молекулярные мишени обходятся столь же дорого, а срок их эффективного воздействия до того, как раковые клетки отреагируют видоизменениями, непродолжителен. Вряд ли можно утверждать, что nivolumab превосходит их по дороговизне, принимая во внимание то, что в результате его применения у многих пациентов наблюдается эффект полной либо существенной ликвидации раковых клеток. В случае, если в Японии применение препарата будет покрываться медицинской страховкой, скорее, это произойдёт в форме его использования в рамках системы покрытия дорогостоящих методов лечения, отчасти снижающей величину расходов, оплачиваемых пациентом из собственного кармана. Тем не менее, бремя бюджетных расходов на нужды медицинского обслуживания возрастёт.
Что же касается задач, которые ещё только предстоит решить, то наряду с пациентами, на которых препарат действует столь результативно, что позволяет им в конце концов прекратить приём лекарств, всё же имеются и случаи, когда препарат оказывается неэффективным. Ответной мерой может послужить начало применения на более ранних сроках. Кроме того, рассматривается возможность разработки маркеров, которые позволили бы заранее определить, будет ли лечение эффективным в том или ином конкретном случае.
Создать «добродетельный круг» взаимосвязи фундаментальных и клинических исследований, университетов и частных предприятий
Препарат nivolumab — это не только плод идеи, подтвердившей себя в ходе первичных клинических испытаний в качестве концепции, пригодной к реализации в товарном продукте, но еще и результат успешного выхода исследований из университетской лаборатории и перехода с фундаментального на клинический уровень.
В нынешнем году 1 апреля в Японии было учреждено национальное Агентство медицинских исследований и разработок (AMED) — один из наиболее важных шагов в рамках так называемой «третьей стрелы абэномики» (стратегия роста за счёт стимулирования частных инвестиций). Уровень японских базовых исследований, в первую очередь, в области индуцируемых плюрипотентных стволовых клеток (iPS-клеток), ничуть не уступает зарубежным странам. Вместе с тем, в стране слаба система реализации результатов таких исследований в плане их клинического использования. Агентство медицинских исследований и разработок призвано стать структурой, которая сосредоточит под единым началом бюджетные ассигнования на проведение исследований и разработок в данной сфере. Оно будет заниматься поддержкой практической реализации успехов, достигаемых в фундаментальных исследованиях, выполняя функции, сопоставимые с задачами Национального института здравоохранения (NIH) в США.
Хондзё Тасуку, которому довелось заниматься исследованиями в NIH, отмечает: «Японским инновациям в области медицины, которые сейчас являются своего рода «билетом в один конец», не хватает подкрепления целенаправленной политикой. Нам необходим механизм возврата в университеты прибыли, получаемой фармацевтическими предприятиями, требуется сформировать добродетельный круг, который позволит университетам готовить за счёт такой обратной связи новые кадры и добиваться новых прорывов». Хочется надеяться, что настоящая взаимосвязь с фармацевтическими предприятиями, обладающими весом на мировом уровне, основанная на принципе обоюдной пользы, позволит в скорейшем времени спасать жизни людей, ежедневно умирающих от онкологических заболеваний.
Фото к заголовку: Хондзё Тасуку (слева) на церемонии вручения учреждённой на Тайване Премии Тан (Tang Prize), 18 сентября 2014 г., Тайбэй (фотография предоставлена Фондом образования Тан)
(Статья на японском языке опубликована 22 апреля 2015 г.)