
Японские исследования iPS-клеток на пути к практическому применению: новые успехи
Наука Технологии- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Использование существующих препаратов контроля иммунитета в борьбе с трудноизлечимыми недугами
iPS-клетки – это клетки, способные преобразовываться в различные виды клеток организма (клетки мышц, костей, сердца, печени, кровеносных сосудов, нервной системы и т. д.), для получения которых достаточно воспользоваться клетками кожи, кровяными и некоторыми другими клетками. Со времени открытия iPS-клеток профессор Яманака наряду с регенеративной медициной отмечал в качестве одного из важнейших направлений клинического применения этих клеток создание лекарственных препаратов, и с сентября 2017 года начались клинические испытания медицинского препарата, предлагаемого в качестве лекарства от трудноизлечимого заболевания – прогрессирующей оссифицирующей фибродисплазии (FOP). Клинические испытания лекарства, открытого с использованием iPS-клеток, проводятся впервые в мире. Этим исследованием занимается заместитель руководителя Центра исследований iPS-клеток Киотского университета Тогутида Дзюнъя.
Прогрессирующая оссифицирующая фибродисплазия – трудноизлечимое генетическое заболевание, которое развивается с детского возраста. У больного по всему телу происходит преобразование в костные ткани грубоволокнистых соединительных тканей – мышц, сухожилий и связок, ограничивая подвижность суставов и деформируя кости. Человек лишается способности нормально питаться, затем затрудняется дыхание, и в конце концов больной умирает. Заболевание редкое – один случай на два миллиона человек, и в стране насчитывается порядка 80 человек с данным диагнозом. Учёные определили гены, вызывающие заболевание, однако эффективного метода его лечения не существует. Заболевание отнесено к числу недугов, лечение которых субсидируется государством.
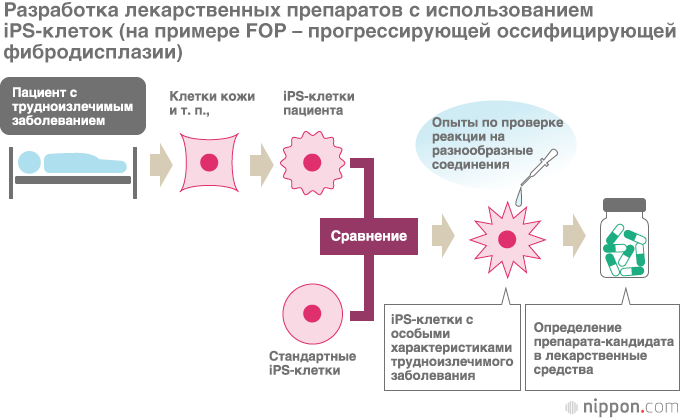
Тогутида Дзюнъя использовал iPS-клетки, полученные из клеток пациентов с данным заболеванием, чтобы выявить вещества, подходящие в качестве лекарства, замедляющего развитие FOP. Сначала удалось добиться успеха в преобразовании взятых у пациента клеток в iPS-клетки. Путем сопоставления этих клеток со стандартными iPS-клетками удалось подтвердить воспроизводство заболевания FOP – заметно более высокую способность к преобразованию в костные и хрящевые клетки, и таким образом прояснить механизм аномального образования костных тканей у больного FOP. Затем, раз за разом наблюдая за реакцией этих iPS-клеток на воздействие различными соединениями, исследовав более 6 800 веществ, удалось обнаружить, что иммуносуппрессант рапамицин обладает нужным эффектом, подавляя преобразование в костные ткани.
Этот препарат используется в Европе для подавления реакции отторжения при проведении операций по пересадке органов (в Японии не одобрен), а в 2014 году препарат был одобрен в Японии в качестве средства для лечения редкого и трудноизлечимого заболевания – лимфангиолейомиоматоза. Такой метод использования уже существующего лекарственного средства в лечении совершенно иного заболевания, называемый переориентацией лекарства (DR), считается весьма безопасным ввиду отсутствия неизвестных побочных эффектов и т. п.
Нынешние клинические испытания, помимо Киотского университета, ведутся в больницах при Токийском университете, а также при университетах Нагои и Кюсю. Двадцать пациентов в возрасте от шести лет и старше разделили на две группы, в одной из которых на протяжении полугода пациенты получают рапамицин. Проверив таким образом его эффективность, исследователи ставят целью добиться одобрения этого препарата в качестве средства для лечения FOP.
Поскольку в случае переориентации уже существующего лекарственного средства проверки на безопасность для человеческого организма уже были проведены, а показатели фармакокинетики проверены на практике, это позволяет радикально снизить сумму издержек по сравнению с разработкой нового лекарства. Но ввиду того, что в случае трудноизлечимых заболеваний, которым подвержено небольшое число людей, фармацевтические компании не могут рассчитывать на получение прибыли, дело сложно довести и до проведения клинических испытаний – процесса, который обходится в сотни миллионов йен. Поэтому в таких случаях с целью расширить сферу применения существующих лекарств клинические испытания под руководством врачей финансируются из государственного бюджета.
Упрощение клинических испытаний безопасности и эффективности
С помощью iPS-клеток, полученных от пациентов с определённым заболеванием (iPS-клеток с присущими заболеванию отличиями) становится возможным воспроизвести особое состояние клеток, характерное именно для данного недуга. Кроме того, это позволяет при проведении проверки лекарственного препарата на безопасность и эффективность не полагаться на опыты на животных, а проделывать необходимую работу, используя такие iPS-клетки.
Появляются надежды на создание лекарств не только для лечения FOP. В Университете Кэйо исследователи под руководством профессора Окано Хидэюки обнаружили препарат, который может послужить лекарством от бокового амиотрофического склероза (болезни Шарко), поражающего двигательные нейроны, и уже в 2018 году планируют приступить к клиническим испытаниям.
Кроме того, профессор Окано и его коллеги обнаружили, что рапамицин способен препятствовать отмиранию клеток внутреннего уха при наследственной глухоте (синдроме Пендреда). К тому же, группа под руководством профессора Фукуды Кэйити в Университете Кэйо обнаружила, что уже существующее лекарство, используемое для лечения лёгочной гипертензии, демонстрирует эффект при гипертрофической кардиомиопатии – наследственном заболевании, при котором происходит утолщение мышечных волокон сердца.
В Центре исследований iPS-клеток Киотского университета группа профессора Цумаки Нориюки обнаружила препарат, который, возможно, можно применять для трудноизлечимых костных заболеваний – хондродистрофии, при которой аномальное формирование клеток хрящевых тканей приводит к малорослости, а также танатофорной дисплазии. Это широко используемое по всему миру средство для понижения уровня холестерина – статин. Исследователи занимаются подтверждением его свойства восстанавливать рост костей.
Выход на этап клинических исследований в регенеративной медицине: глазная сетчатка, сердечная мышечная ткань и др.
В регенеративной медицине, которая является ещё одним важным направлением клинического использования iPS-клеток, в 2013 году Институт физико-химических исследований RIKEN в рамках проекта под руководством Такахаси Масаё приступил к клиническим исследованиям метода лечения трудноизлечимой возрастной макулодистрофии, использующего клетки, полученные из iPS-клеток. Вслед за этим в Осакском университете профессор Сава Ёсики (генеральный директор Японского научного общества регенеративной медицины) в ближайшем будущем намеревается приступить к клиническим опытам по пересадке пациентам с тяжёлыми заболеваниями сердца сердечных мышечных тканей, изготовленных из iPS-клеток. Эта разработка была проведена совместно с корпорацией Terumo.
Уже упомянутый профессор Окано Хидэюки из Университета Кэйо также ведёт подготовку к пересадке пациентам с повреждениями спинного мозга нейрональных стволовых клеток, полученных путём преобразования iPS-клеток. Кроме того, профессор Такахаси Дзюн из центра исследований iPS-клеток Киотского университета в августе 2017 года объявил о том, что в результате пересадки обезьяне с симптомами болезни Паркинсона нервных клеток, полученных из iPS-клеток, произошло ослабление дрожания верхних и нижних конечностей, а также других симптомов. Впервые подтвердив эффект на близких к человеку приматах, исследователи ставят целью приступить к клиническим опытам уже в 2018 финансовом году.
В более отдалённой перспективе исследователи мечтают создавать целиком отдельные жизненно важные органы. Профессор Сава Ёсики, говоря о регенеративной медицине через 30 лет, отметил: «Если речь идёт о таких органах с простыми функциями, как, к примеру, сердце, чья работа состоит в сжатии – возможно, мы сможем создавать такие органы целиком».
В Центре исследований iPS-клеток, который возглавляет профессор Яманака Синъя, в 2013 году начали работу по созданию банка iPS-клеток из материала людей, чей тип иммунитета отличает слабость реакции отторжения, и уже в 2017 году этот банк будет состоять из iPS-клеток типов, подходящих для 30 процентов японцев. Банк будет поставлять эти iPS-клетки и для клинических опытов по лечению возрастной макулодистрофии, а также по пересадке сердечных мышечных тканей. Вместе с тем на пути к клиническому использованию, опираясь на фундаментальные исследования iPS-клеток, предстоит решить целый ряд задач, главные из которых – предотвращение преобразования в раковые клетки, повышение качества клеточного материала и преобразование в клетки различных органов.
Фотография к заголовку: профессор Осакского университета Сава Ёсики на пресс-конференции после подачи заявки на проведение клинических исследований лечения сердечной недостаточности с использованием iPS-клеток, 21 июля 2017 г., преф. Осака, город Суйта (фотография предоставлена Jiji Press)
(Статья на японском языке опубликована 12 октября 2017 г.)