Япония одобрила первые в мире медицинские продукты на основе iPS-клеток
Новости
Наука- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Токио, 6 марта (Jiji Press) — Министерство здравоохранения, труда и социального обеспечения Японии 6 марта объявило, что условно одобрило производство и продажу двух регенеративных медицинских продуктов на основе индуцированных плюрипотентных стволовых клеток (iPS-клеток). Это первое в мире одобрение медицинских продуктов с использованием iPS-клеток.
Одобрение получили сердечная мышечная клеточная пластина «ReHeart» для пациентов с сердечными заболеваниями, разработанная токийской венчурной компанией Cuorips, основанной при Университете Осаки, а также допаминергические нервные клетки «Amchepry» для пациентов с болезнью Паркинсона, созданные фармацевтической компанией Sumitomo Pharma (Осака).
После подачи компаниями соответствующих заявок эти продукты, как ожидается, будут включены в систему государственного медицинского страхования и смогут использоваться в рамках страхового лечения.
Обе компании в течение следующих семи лет будут дополнительно собирать данные, в том числе об эффективности. Cuorips планирует изучить результаты лечения 75 пациентов препаратом «ReHeart», а Sumitomo Pharma — 35 пациентов препаратом «Amchepry», после чего вопрос об окончательном одобрении будет рассмотрен повторно.
В феврале специализированный комитет министерства уже одобрил эти продукты в рамках системы условного и ограниченного по сроку разрешения. Министр здравоохранения Уэно Кэнъитиро на пресс-конференции после заседания кабинета 6 марта заявил, что надеется, что они «станут спасением для пациентов во всём мире».
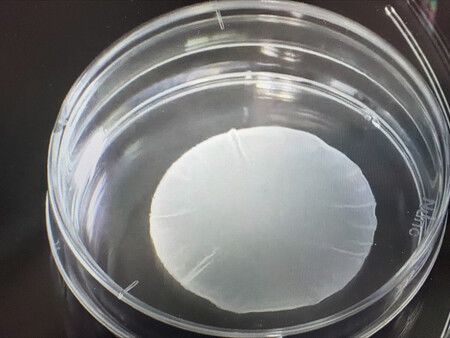
«ReHeart» представляет собой пластину диаметром 4–5 сантиметров и толщиной около 0,1 миллиметра, изготовленную из сердечных мышечных клеток, полученных из iPS-клеток. Её прикрепляют к сердцу пациента для восстановления его функции.
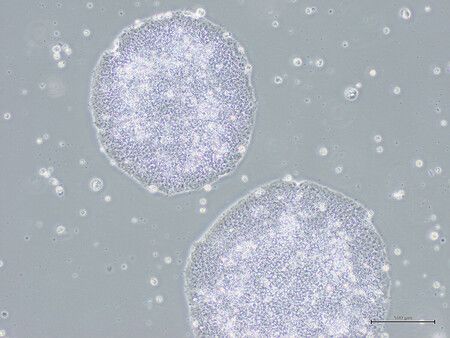
«Amchepry» предполагает пересадку от 5 до 10 миллионов нервных клеток в центральную часть головного мозга с целью улучшения двигательных функций.
По данным Cuorips, компания планирует начать продажи в Японии примерно этой осенью, а также ускорить работу по выходу на зарубежные рынки. Sumitomo Pharma намерена провести послерегистрационные клинические испытания в семи медицинских учреждениях; первую трансплантацию планируется провести примерно в октябре—декабре этого года. После этого в течение двух лет будут проверяться эффективность и безопасность препарата.
[Авторское право The Jiji Press, Ltd.]
Jiji Press iPS-клетки болезнь Паркинсона регенеративная медицина сердечная недостаточность